7 - On réalise un circuit en série simple pour tester le caractère conducteur de différents solides placés entre les pinces crocodiles. Les résultats de l'expérience sont présentés dans le tableau suivant.
Parmi les affirmations suivantes, lesquelles (laquelle) peut-on déduire de cette expérience ?
(plusieurs réponses possibles)

1. Tous les solides sont conducteurs.
2. L'acier est conducteur, car il est formé de fer et de carbone graphite.
3. Le caoutchouc est un isolant.
4. Le carbone graphite est un métal.
5. Tous les métaux conduisent le courant.
8 - On réalise un circuit en série simple pour tester le caractère conducteur de différentes solutions placées dans un électrolyseur. Les résultats de l'expérience sont présentés dans le tableau suivant.
Parmi les affirmations suivantes, lesquelles (laquelle) peut-on déduire de cette expérience ?
(plusieurs réponses possibles)

1. En dissolvant du sel dans de l'eau pure, cette eau devient conductrice.
2. L'eau du robinet est une solution conductrice.
3. Le sel conduit le courant.
4. Pour que l'eau du robinet soit isolante, il suffit d'y dissoudre du sucre.
5. L'eau minérale est une eau pure, puisqu'elle n'est jamais trouble.
9 - Parmi les affirmations suivantes, lesquelles (laquelle) peut-on déduire de cette expérience ?
(plusieurs réponses possibles)
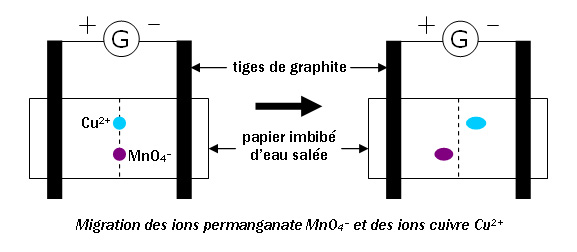
1. Les ions permanganate sont de couleur violette.
2. L'eau salée est conductrice.
3. Les ions permanganate sont attirés par le pôle négatif du générateur.
4. Si on poursuit l'expérience, les ions cuivre vont atteindre les tiges de graphite et conduire le courant dans les fils de connexion.
5. Les ions cuivre et permanganate se déplacent parce qu'ils sont poussés par les électrons qui font passer le courant dans le papier.
10 - Parmi les affirmations suivantes, lesquelles (laquelle) peut-on déduire de cette expérience ?
(plusieurs réponses possibles)
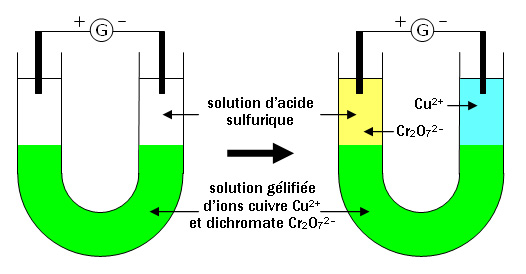
1. L'acide sulfurique est jaune.
2. Les ions cuivre sont positifs et se déplacent vers le pôle négatif du générateur et c'est l'inverse pour les ions dichromate.
3. Dans la zone verte, le courant se déplace grâce à des électrons.
4. Les ions cuivre sont de couleur bleue.
5. Lorsque les ions arrivent au contact des tiges de graphite, ce sont les électrons qui assurent la conduction du courant.
11 - Parmi les informations suivantes, laquelle(lesquelles) est(sont) correcte(s) ?
(plusieurs réponses possibles)
1. Dans un métal, la conduction du courant est assurée par le déplacement des ions et des électrons.
2. Dans une solution, la conduction du courant est assurée par le déplacement des ions uniquement.
3. Les électrons d'un métal se déplacent du pôle négatif vers le pôle positif à l'extérieur du générateur : c'est le sens réel du courant.
4. Les électrons d'un métal se déplacent du pôle positif vers le pôle négatif à l'extérieur du générateur : c'est le sens réel du courant.
5. Dans un isolant la conduction du courant est assurée par le déplacement des électrons uniquement.
12 - Parmi les informations suivantes, laquelle(lesquelles) est(sont) correcte(s) ?
(plusieurs réponses possibles)
1. Un atome est essentiellement constitué de vide.
2. Un atome est constitué d'un noyau, d'un ion et d'électron(s).
3. Les électrons et les ions sont chargés électriquement.
4. Un ion est un atome qui a gagné ou perdu un ou plusieurs électrons.
5. Les atomes et les molécules sont électriquement neutres.
13 - Selon le texte, laquelle(lesquelles) des affirmations suivantes est(sont) correcte(s) ?
(plusieurs réponses possibles)

1. Le modèle de Rutherford est appelé 'modèle planétaire' car tout le monde sur Terre va adopter ce modèle.
2. Un atome a la forme d'une boule dont le volume est entièrement occupé par des électrons et un noyau.
3. On parle de nuage d'électrons parce qu'on ne sait pas exactement où ils sont autour du noyau, par comparaison avec les microgouttelettes d'eau invisibles qui composent un nuage.
4. Entre la taille de l'atome et la taille du noyau, il y a un rapport de 10 à la puissance 6.
5. Dans un atome il y a autant de charges négatives que de charges positives, mais la masse de l'atome est concentrée dans ses électrons.
14 - Choisis la réponse correcte à la question suivante.
(tu peux t'aider d'un papier et d'un stylo)
(une seule réponse possible)

A
B
C
D
E
15 - Un atome de chlore possède 17 charges positives sur son noyau. Combien possède-t-il de charges négatives ?
(une seule réponse possible)
17
18
19
1
aucune
16 - Un atome de sodium possède 11 charges positives sur son noyau. Combien possède-t-il d'électrons ?
(une seule réponse possible)
10
1
15
11
aucun
17 - Un atome de fer possède 26 électrons. Combien possède-t-il de charges positives sur son noyau ?
(une seule réponse possible)
26
1
28
13
aucun
18 - Un atome d'aluminium possède 13 charges négatives.
Si cet atome d'aluminium perd 3 électrons, combien de charges négatives l'ion aluminium obtenu possède-t-il ?
(une seule réponse possible)
13
10
16
8
1
19 - Un atome de potassium possède 19 électrons.
Si cet atome de potassium gagne 1 électron, combien de charges négatives l'ion obtenu possède-t-il ?
(une seule réponse possible)
10
18
1
20
aucun
20 - Un atome de fluor possède 9 charges électriques positives dans son noyau.
Si cet atome de fluor gagne 1 charge négative, combien de charges négatives l'ion obtenu possède-t-il ?
(une seule réponse possible)
10
9
8
1
aucun
21 - Un atome de calcium possède 20 charges électriques positives dans son noyau. Si cet atome de fluor perd 2 électrons, combien de charges négatives l'ion obtenu possède-t-il ?
(une seule réponse possible)
18
20
22
10
aucun
22 - Un atome de soufre S possède 16 charges électriques positives dans son noyau. Si cet atome de soufre gagne 2 électrons, quelle est la formule chimique de l'ion obtenu ?
(une seule réponse possible)
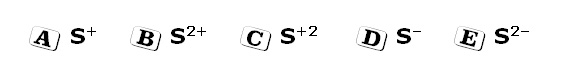
A
B
C
D
E
23 - Un atome de lithium Li possède 3 charges électriques positives dans son noyau. Si cet atome de lithium perd 1 électron, quelle est la formule chimique de l'ion obtenu ?
(une seule réponse possible)

A
B
C
D
E
Si vous souhaitez envoyer vos résultats par courrier
électronique, cliquez
Ce questionnaire a été réalisé avec Questy